Obsah
Protony, neutrony a elektrony jsou tři hlavní částice, které tvoří atom. Jak jejich názvy napovídají, první jsou kladně nabité, druhé nemají žádný náboj (jsou neutrální) a třetí mají záporný náboj. Elektrony mají velmi malou hmotnost, zatímco protony a neutrony mají téměř identickou hmotnost. Počet každého z nich v atomu najdete pouze pomocí informací z periodické tabulky.
Kroky
Část 1 ze 2: Výpočet protonů, elektronů a neutronů
Získejte periodickou tabulku. Je to obrázek, který organizuje prvky podle atomové struktury. Je klasifikován podle barev a dává každému prvku jedinečnou zkratku jednoho, dvou nebo tří písmen. Další informace zahrnují atomovou hmotnost a počet.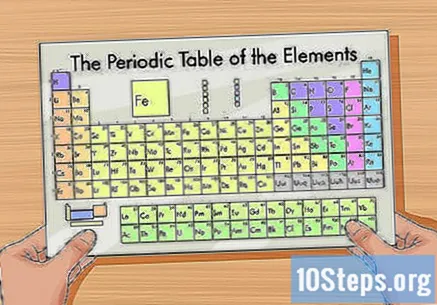
- Periodickou tabulku najdete online nebo v knize o chemii.
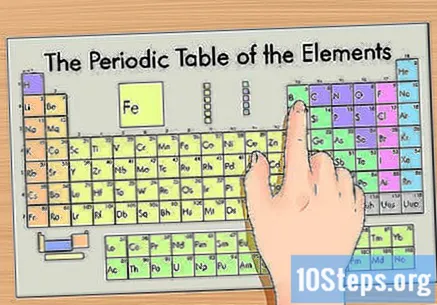
Najděte svůj prvek v periodické tabulce. Organizuje prvky podle atomového čísla a rozděluje je do tří hlavních skupin: kovy, nekovy a metaloidy (polokovy). Mezi další skupiny patří alkalické kovy, halogeny a vzácné plyny.- Použití skupiny (sloupce) nebo tečky (řádky) může usnadnit vyhledání prvku v tabulce.
- Symbol prvku můžete také vyhledat, pokud neznáte žádné další vlastnosti.
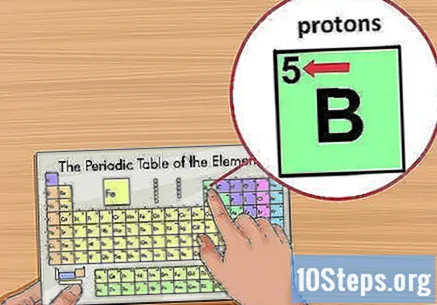
Vyhledejte atomové číslo. Je umístěn nad symbolem prvku v levém horním rohu čtverce. Atomové číslo vám řekne, kolik protonů tvoří jeden atom daného prvku.- Například Bor (B) má atomové číslo 5, a tedy pět protonů.
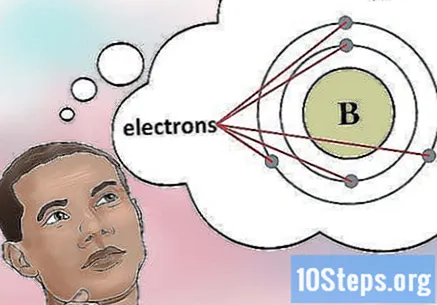
Určete počet elektronů. Protony jsou částice v jádru atomu, které mají kladný náboj. Elektrony jsou záporně nabité částice. Proto bude mít neutrální prvek stejný počet protonů a elektronů.- Například Bor (B) má atomové číslo 5, a tedy pět protonů a pět elektronů.
- Pokud však prvek obsahuje kladný nebo záporný iont, protony a elektrony nebudou stejné. Budete je muset vypočítat. Iontové číslo se po prvku zobrazí jako malý horní index.
Hledejte atomovou hmotnost. Chcete-li zjistit počet neutronů, musíte nejprve najít atomovou hmotnost. Tato hodnota je průměrná hmotnost atomů prvku a lze ji najít pod symbolem prvku.
- Zaokrouhlete atomovou hmotnost na další celé číslo. Například atomová hmotnost boru je 10 811, ale můžete ji zaokrouhlit až na 11.
Odečtěte atomové číslo od atomové hmotnosti. Chcete-li zjistit počet neutronů, musíte odečíst atomové číslo od hmotnosti. Pamatujte, že atomové číslo je stejné jako u protonů, které již byly identifikovány.
- Pro náš příklad boru 11 (atomová hmotnost) - 5 (atomové číslo) = 6 neutronů
Část 2 ze 2: Výpočet elektronů s přítomnými ionty
Určete počet iontů. Po prvku se zobrazí jako malá hodnota horního indexu. Ion je atom s kladným nebo záporným nábojem z důvodu přidání nebo odstranění elektronů. V iontu zůstává počet protonů stejný, ale počet elektronů se mění.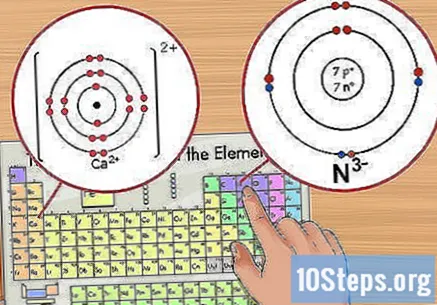
- Jelikož má elektron záporný náboj, je po jeho odstranění iont kladný. Jak se přidává více elektronů, iont se stává záporným.
- Například N má náboj -3, zatímco Ca náboj +2.
- Nezapomeňte, že tento výpočet nemusíte provádět, pokud za prvkem není žádné horní indexové číslo.
Odečtěte náboj od atomového čísla. Když má iont kladný náboj, ztratil atom elektrony. Chcete-li vypočítat zbývající množství z nich, odečtěte částku dodatečného náboje od atomového čísla. V případě kladného iontu existuje více protonů než elektronů.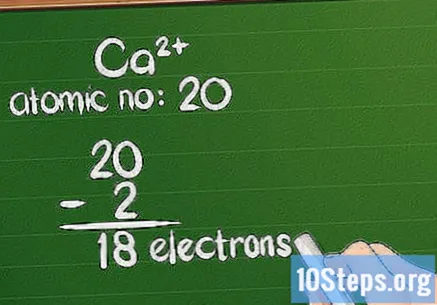
- Například Ca má náboj +2, takže ztratil 2 elektrony ze svého přirozeného stavu. Atomové číslo vápníku je 20, takže ion má 18 elektronů.
Přidejte náboj k atomovému číslu záporných iontů. Když má ion negativní náboj, získal atom elektrony. Chcete-li vypočítat jejich celkový počet, jednoduše přidáte částku extra poplatku k atomovému číslu. V případě záporného iontu je méně protonů než elektronů.
- Například N má náboj -3, takže ve srovnání s neutrálním stavem získal tři elektrony. Atomové číslo dusíku je 7, takže tento iont má 10 elektronů.