Obsah
V chemii elektronegativita je to míra přitažlivosti, kterou atom působí na elektrony ve vazbě. Atom s vysokou elektronegativitou přitahuje elektrony s velkou intenzitou, zatímco atom s nízkou elektronegativitou to provede s malou intenzitou. Tyto hodnoty se používají k predikci toho, jak se budou různé atomy chovat, když jsou navzájem spojeny, což činí toto téma důležitou dovedností v základní chemii.
Kroky
Metoda 1 ze 3: Základní pojmy elektronegativity
Pochopte, že k chemickým vazbám dochází, když atomy sdílejí elektrony. Pro pochopení elektronegativity je důležité nejprve pochopit, co je to „odkaz“. Jakýkoli dva atomy v molekule „navzájem spojené“ v molekulárním diagramu jsou označeny jako vazby mezi nimi. V podstatě to znamená, že sdílejí sadu dvou elektronů - každý atom přispívá atomem k vazbě.
- Přesné důvody, proč atomy sdílejí elektrony a vazby dohromady, neodpovídají zaměření tohoto článku. Pokud se chcete dozvědět více, hledejte na internetu základní pojmy chemických vazeb.
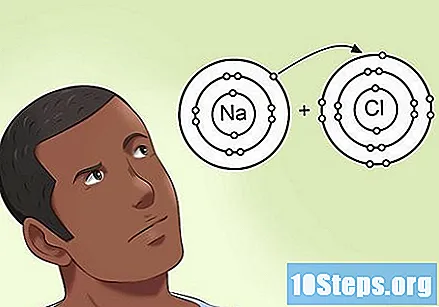
Pochopte, jak elektronegativita ovlivňuje elektrony přítomné ve vazbě. Když dva atomy sdílejí soubor dvou elektronů ve vazbě, není mezi nimi vždy stejné sdílení. Když má jeden z nich vyšší elektronegativitu než atom, ke kterému je připojen, přiblíží oba elektrony k sobě. Atom s velmi vysokou elektronegativitou může elektrony přitáhnout na stranu ve vazbě a téměř zrušit sdílení s ostatními.- Například v molekule NaCl (chlorid sodný) má atom chloru vysokou elektronegativitu a sodík, nízkou elektronegativitu. Brzy budou elektrony staženy směrem k chloru a od sodíku.

Jako referenční použijte tabulku elektronegativity. Tabulka elektronegativity představuje prvky uspořádané přesně jako periodická tabulka, ale každý atom je označen svou elektronegativitou. Najdete je v několika učebnicích chemie, v odborných článcích a také na internetu.- Zde je vynikající tabulka elektronegativity. Všimněte si, že používá Paulingovu elektronegativitu, což je běžnější. Existují však i jiné způsoby měření elektronegativity, z nichž jeden bude uveden níže.
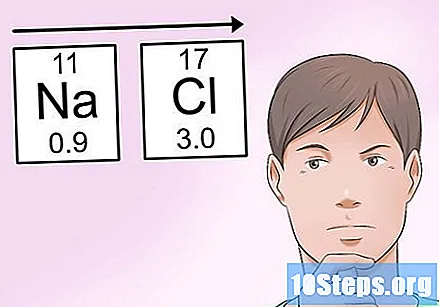
Nezapomeňte na trendy elektronegativity, abyste mohli snadno odhadovat. Pokud nemáte k dispozici tabulku elektronegativity, je stále možné odhadnout tuto hodnotu na základě vaší polohy v periodické tabulce. Jako obecné pravidlo:- Elektronická aktivita atomu zvyšuje při přechodu na že jo v periodické tabulce.
- Elektronická aktivita atomu zvyšuje jak se pohybujete nahoru v periodické tabulce.
- Atomy v pravém horním rohu tedy mají nejvyšší hodnoty elektronegativity a atomy v levém dolním rohu mají nejnižší.
- Například v předchozím příkladu NaCl můžete určit, že chlor má vyšší elektronegativitu než sodík, protože je téměř na nejvyšším pravém bodě. Na druhé straně je sodík daleko nalevo od stolu, což z něj činí jeden z nejméně cenných atomů.
Metoda 2 ze 3: Hledání spojení s elektronegativitou
Najděte rozdíl v elektronegativitě mezi dvěma atomy. Když jsou dva atomy spojeny dohromady, rozdíl mezi jejich hodnotami elektronegativity odhalí hodně o kvalitě této vazby. Odečtěte nejmenší hodnotu od největší k nalezení rozdílu.
- Pokud se například podíváme na molekulu HF, odečteme hodnotu elektronegativity vodíku (2.1) od hodnoty fluoru (4.0). 4,0 - 2,1 = 1,9.
Pokud je rozdíl pod 0,5, je vazba kovalentní a nepolární. Zde jsou elektrony sdíleny téměř stejně. Tyto vazby netvoří molekuly s velkými rozdíly v náboji na obou koncích. Polární vazby jsou často velmi obtížné rozbít.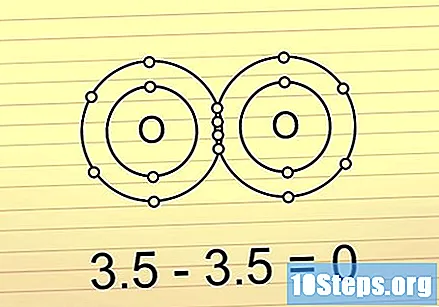
- Například molekula O2 představuje tento typ připojení. Protože dvě molekuly kyslíku mají stejnou elektronegativitu, rozdíl mezi nimi je roven 0.
Pokud je rozdíl mezi 0,5 a 1,6, je vazba kovalentní a polární. Tyto svazky drží více elektronů na jednom konci než na druhém konci. Toto dělá molekulu trochu více negativní na konci s více elektrony a trochu více pozitivní na konci bez nich. Nerovnováha náboje v těchto vazbách umožňuje molekulám účastnit se některých specifických reakcí.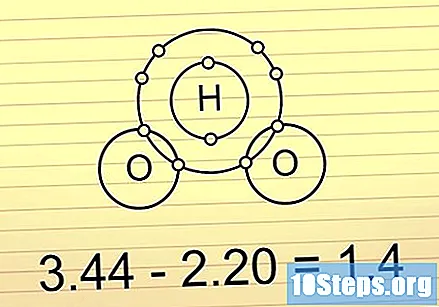
- Dobrým příkladem je molekula H2O (voda). O je více elektronegativní než dvě H, takže udržuje elektrony blíže a činí celou molekulu částečně negativní na O konci a částečně pozitivní na H zakončení.
Pokud je rozdíl větší než 2, je vazba iontová. V těchto svazcích jsou elektrony umístěny zcela na jednom konci. Nej elektronegativnější atom získá záporný náboj a nejméně elektronegativní atom získá kladný náboj. Tento typ vazby umožňuje atomům reagovat s jinými atomy nebo je dále oddělit polárními atomy.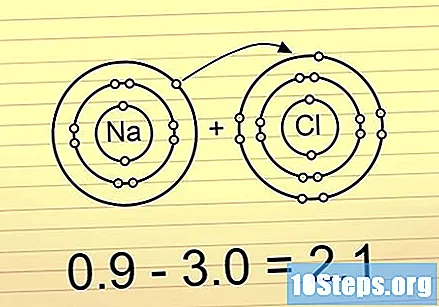
- Příkladem toho je NaCl (chlorid sodný). Chlor je tak elektronegativní, že přitahuje oba elektrony z vazby k sobě, takže sodík má kladný náboj.
Pokud je rozdíl mezi 1,6 a 2, hledejte kov. Li tam kov přítomný ve vazbě, to znamená, že je iontový. Pokud existují jiné nekovy, vazba je polární kovalent.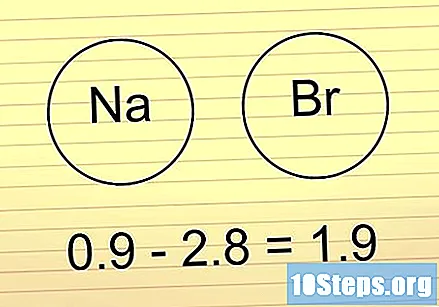
- Kovy obsahují většinu atomů vlevo a uprostřed periodické tabulky. Tato stránka obsahuje tabulku ukazující, které prvky jsou kovy.
- Náš předchozí příklad HF spadá do této skupiny. Protože H a F nejsou kovy, vazba bude polární kovalent.
Metoda 3 ze 3: Objevte elektronegativitu Mulliken
Najděte první ionizační energii svého atomu. Mullikenova elektronegativita sestává z metody měření mírně odlišné od metody uvedené v Paulingově tabulce výše. Chcete-li najít jeho hodnotu pro daný atom, najděte svou první ionizační energii. Toto je energie potřebná k tomu, aby se atomový výboj stal jediným elektronem.
- Tuto hodnotu lze pravděpodobně nalézt v chemických referenčních materiálech. Tato stránka obsahuje dobrou tabulku, kterou můžete použít (najděte ji dolů).
- Řekněme například, že chcete zjistit, jaká je elektronegativita lithia (Li). V tabulce na výše uvedené stránce vidíme, že první ionizační energie je ekvivalentní 520 kJ / mol.
Zjistěte, jaká je elektronová afinita atomu. Toto je měření energie získané, když je elektron přidán k atomu za vzniku záporného iontu. To je opět něco, co by se mělo nalézt v referenčních materiálech. Tato stránka obsahuje zdroje, které mohou být užitečné.
- Elektronická afinita k lithiu je stejná 60 kJ mol.
Vyřešte Mullikenovu rovnici elektronegativity. Při použití kJ / mol jako energetické jednotky lze Mullikenovu rovnici elektronegativity napsat jako ENMulliken = (1,97 × 10) (Ei + Ea) + 0,19. Vložte známá data do rovnice a najděte hodnotu ENMulliken.
- V našem příkladu dosáhneme následujícího usnesení:
- ENMulliken = (1,97 × 10) (Ei + Ea) + 0,19
- ENMulliken = (1,97 × 10)(520 + 60) + 0,19
- ENMulliken = 1,143 + 0,19 = 1,333
- V našem příkladu dosáhneme následujícího usnesení:
Tipy
- Kromě škály Pauling a Mulliken existují i jiné váhy elektronegativity, jako jsou Allred-Rochow, Sanderson a Allen. Každá z nich má své vlastní rovnice pro výpočet elektronegativity (a některé z nich mohou být docela složité).
- Elektronegativita nemá měrnou jednotku.